صادق اسفیدان
بسم الله الرحمن الرحیم سایت شخصی صادق قربانی اسفیدانصادق اسفیدان
بسم الله الرحمن الرحیم سایت شخصی صادق قربانی اسفیدانروش رسم دیاگرام دو فازی
رسم نمودار فازی
بخش اول
چگونه یک نمودار فازی رسم کنیم:
یک دیاگرام فازی دوتایی نشان دهنده فازهای تشکیل شده و موجود در درصدهای مختلف از
مخلوط دو عنصر و در یک دامنه دمایی می باشد.
ترکیب شیمیایی از ۱۰۰ درصد در مورد عنصر A در سمت چپ نمودار آغاز و با در نظر گرفتن تمامی
مخلوطهای ممکن به ۱۰۰ درصد از عنصر B در سمت راست پایان می یابد.

ترکیب شیمیایی یک آلیاژ به شکل A - x%B نشان داده می شود. برای نمونه Cu - 20%Al دارای ۸۰ درصد مس و ۲۰ درصد آلومینیوم می باشد.
برای نشان دادن خواص عناصر آلیاژی معمولا از درصد وزنی (Weight percentage ) استفاده می شود از درصد اتمی ( Atomic percentage ) هم می توان استفاده نمود.د درصد وزنی با wt% و درصد اتمی باا at%نشان داده می شود. در این نوشته ما از درصد وزنی استفاده می کنیم.
تفاوت درصد وزنی و اتمی را با یک مثال نشان می دهیم:
وقتی از Cu-27at%Al حرف می زنیم، یعنی در این آلیاژ ۲۷% اتمها مربوط به آلومینیوم و ۷۳ % اتمها مس هستند و هنگامی که آلیاژ به شکل Cu-27wt%Al باشد، ۲۷% از وزن آلیاژ Al و ۳۷% Cu خواهد بود.
__________________
رسم نمودار فازی بخش دوم
تمایل در آلیاژها انجماد در یک دامنه دمایی (به جای انجماد در دمایی خاص مانند آنچه در
عناصر خالص رخ می دهد)، می باشد.
در هر یک از دو سر نمودار فازی فقط یکی از عناصر (۱۰۰% A یا ۱۰۰%B) و در
نتیجه یک نقطه ذوب خاص وجود دارد.
در برخی مواقع نیز مخلوطهایی وجود دارند که مانند عناصر خالص در یک دمای ویژه منجمد می
شوند. این نقطه به نام نقطه یوتکتیک نامیده می شود. امکان وجود بیش از یک نقطه
یوتکتیک در برخی نمودار های فازی وجود دارد. نقطه یوتکتیک نقطه ای است که واکنش
یوتکتیک رخ می دهد.

نقطه یوتکتیک را می توان به صورت تجربی با رسم نمودارهای نرخ سرد شدن در دامنه ای از ترکیب شیمیایی آلیاژ به دست آورد.
این نمودار ساده فازی معمولا فقط وقتی بوجود می آید که دو عنصر بسیار شبیه به هم تشکیل آلیاژی را داده و یا بخشی از یک نمودار فازی پیچیده باشند
رسم نمودار فازی بخش سوم
با سرد کردن آلیاژ از حالت مذاب و ثبت کردن نرخ سرد شدن آن، می توان دمای شروع انجماد را مشخص و در نمودار فازی رسم نمود. با انجام دادن آزمایشات تجربی به تعداد کافی در دامنه ای از ترکیب شیمیایی، یک منحنی شروع انجماد را در نمودار می توان رسم نمود. این منحنی به سه نقطه انجماد ساده (Single) ختم می شود و به خط لیکیدوس معروف است. بالای این خط فقط حالت مایع از آلیاژ وجود خواهد داشت.
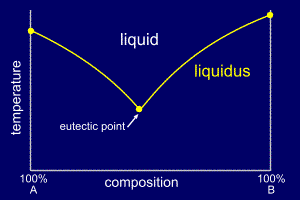
به همان روشی که شکر در چای داغ حل می شود(محلول مایع)، برای یک عنصر نیز امکان اینکه در یک عنصر
دیگر حل شده ،در حالی که هر در حالت جامد باقی بمانند، وجود دارد. به این امر حلالیت جامد می گویند
که مشخصاً تا چند درصد وزنی وجود دارد.
این حد حلالیت معمولا با دما تغییر می کند.
گستردگی منطقه حلالیت جامد را می توان در نمودار فازی رسم کرده و نامگذاری نمود. محلول جامدی از عنصر Bدر A(یعنی عمدتا عنصر A وجود داشته باشد)، به نام فاز آلفا(فاز تشکیل شده در سمت چپ نمودار) و وارون این حالت بتا (فاز تشکیل شده در سمت راست نمودار)نامیده می شود.
نکته قابل توجه در در مورد برخی از عناصر این است که برخی از این عناصر در حالت آلیاژی با یکدیگر دارای حلالیت صفر هستند(در همدیگر حل نمی شود). یک شاهد بسیار خوب آلیاژ های Al – Si است که آلومینیوم در سیلیکون حلالیت برابر با صفر دارد.
 __________________
__________________
رسم نمودار فازی بخش چهارم
اگر ترکیب شیمیایی یک آلیاژ در منطقه کوچک محلول جامد و یا در کناره های نمودار فازی قرار نگیرد، آلیاژ
در نقطه یوتکتیک به شکل کامل جامد می شود که این به شکل خط یوتکتیک در نمودار فازی نشان داده شده است.
در دماها و ترکیبات شیمیایی بین شروع انجماد و نقطه ای که جامد کامل به دست می
آید(دمای یوتکیتیک)، مخلوطی خمیری
از هر دو فاز آلفا یا بتا به شکل توده های جامد با مخلوطی مایع از A و B بوجود خواهد آمد. این منطقه را که به صورت
جزیی جامد شده است، در نمودار فازی زیر می توانید مشاهده کنید.
منطقۀ قرار گرفته در زیر خط یوتکتیک و خارج از منطقۀ محلول جامد، مخلوطی از آلفا و بتا خواهد بود

خطوط ارتباطی و قانون اهرم Lever
آلیاژی را که در نمودار زیر نشان داده شده است، در دما و ترکیب مشخص ده در نظر
بگیرید. در این دما آلیاژ مخلوطی از فازهای آلفا و مایع(مذاب) است اما ترکیب دقیق
شیمیایی در این دما چیست؟
یک خط ایزوترمال(دمای ثابت) از نقطه مورد نظر رسم کنید. این خط دو منحنی حلالیت مجاورش را قطع می کند و به نام خط ارتباطی نامیده می شود(Tie Line). دوسر انتهایی این خط نشان دهنده ترکیب شیمیایی دو فاز موجود در حالت تعادل با دیگر فاز در این دما می باشد.
از نمودار می دانیم که فازهای آلفا و مذاب وجود دارند. خط ارتباطی نشان می دهد که فاز آلفا ۵/۲% B و فاز مذاب ۳۴/۵%B در این دما است. توجه داشته باشید که ترکیب کلی نمونه بدون تغییر مانده و ما فقط ترکیب شیمیایی فازهای تشکیل دهنده نمونه را تعیین می کنیم.

برای یک آلیاژ که در ترکیب شیمیایی Co و دمای Tx سرد شده است، خطوط ارتباطی برای جواب دادن به پرسشهای زیر بکار می رود:
-چه فازهایی وجود دارند؟
- ترکیب شیمیایی آنها چیست؟
- اگر دما تا Ty کاهش یابد، ترکیب شیمیایی دو فاز چگونه تغییر می کند؟
چون ترکیب شیمیایی Co و دمای Tx در منطقه فازی بتا + مذاب همدیگر را قطع می کنند، بنابراین فاز بتا و مذاب فازهای موجود هستند.
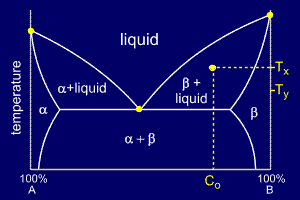
پاسخ پرسش دوم دربارۀ ترکیب شیمیایی:
بایستی خطی افقی از نقطه مورد نظر به نزدیکترین مرزهای نمودار فازی رسم کرد. این خط نشان دهنده موارد زیر خواهد بود:
<!--[if !supportLists]-->- <!--[endif]-->مذاب: X درصد وزنی از B
<!--[if !supportLists]-->- <!--[endif]-->فاز بتا: Y درصد وزنی B
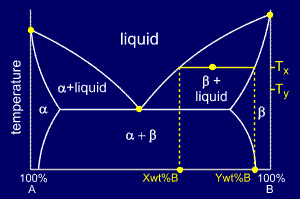
با کاهش دما تا Ty خط جدیدی از نقطه مورد نظر که از تقاطع این دما و ترکیب شیمیایی به دست می آید، رسم کنید.
ترکیب شیمیایی عبارتست از:
<!--[if !supportLists]-->- <!--[endif]-->مذاب: X’ درصد وزنی از B
<!--[if !supportLists]-->- <!--[endif]-->فاز بتا: Y’ درصد وزنی B
بنابراین، هر دو فاز مذاب و بتا وقتی نمونه سرد شود،غنی تر از عنصر A می شود.
اکنون ما ترکیب شیمیایی دو فاز را می دانیم و نیاز به این داریم دریابیم که چه مقدار از هر فاز در دمای داده شده وجود دارد.
نسبت کسری از هر دو فاز را بوسیله قانون اهرم Lever می توان به دست آورد.
در نگاه اول این قانون گیج کننده به نظر می رسد. در واقع این قانون تبدیل جرم بوده و می توان آن را به شکل ریاضی تبدیل کرد.
ما ابتدا با یک ترکیب شیمیایی کلی Co آغاز کردیم. از خط ارتباطی رسم شده دریافتیم که دو فاز موجود در یک دمای خاص دو ترکیب شیمیایی مختلف دارند، اما مقدار کلی این دو ترکیب شیمیایی بایستی به مقدارترکیب کلی آلیاژ اضافه شود. این اساس قانون اهرم است.

 __________________
__________________
mamnon az matlabeton
لطفا منبع این مطلب را ذکر می کنید.وچه کتابی در ارتباط با خطوط ایزوترمال پیشنهاد می کنید برای تکمیل این بحث
باسلام میشه این سوالات پاسخ دهید
1. در اینجا چرا خطوط گرهی موازی محور x هست؟
2.مقدار درجه ازادی در دمای بحرانی Tc چند است و معناش چیست؟؟؟